Genel olarak sularda sertlik denildiğinde, yalnızca kalsiyum düzeyi akla gelmektedir. Oysa suyun sertliği kavramı ile kalsiyum (Ca++) ve magnezyum (Mg++) iyonlarının toplamı anlaşılır ve 1 litre suyun içerdiği kalsiyum oksit (CaO) ve kalsiyum karbonat (CaCO3) şeklinde belirtilir.
Doğal kaynaklardan çıkan su havadan karbondioksiti alarak asidik özellik kazanır. Böyle bir su örneği magnezyum ve kalsiyum tuzlarından oluşan kayalarla temasa geçince onların içindeki tuzları çözer. Magnezyum ve kalsiyum iyonlarını içeren suya “sert su” denir.
Eğer sodyum ve potasyum bileşikli sabunlar bu tür bir suya eklenirse, sodyum ve potasyum iyonları magnezyum ve kalsiyum iyonları ile yer değiştirerek çökelek oluşumuna neden olurlar. Bu durum sertliğe neden olan iyonların tümünün çökmesine kadar devam eder. Ortamda bulunan magnezyum ve kalsiyum iyonlarının hepsi çöktükten sonra sabun köpürmeye başlar. Suyun asitlik derecesi fazla olursa sodyum ve potasyum sabunları parçalanarak serbest yağ asitlerine dönüşürler. Bu nedenle su sertliği giderilirken su içerisinde varsa bu tür asitlerin de giderilmesi gerekir.
Çeşitli sertlik birimleri vardır. Bunlardan en çok kullanılanları şunlardır:
Fransız Sertlik Derecesi (FS): 100 ml suda çözünmüş olarak bulunan sertlik veren maddelerin, 1mg kalsiyum karbonat (CaCO3) miktarına karşılık gelen madde miktarına denir. 0f sembolü ile gösterilir.
İngiliz Sertlik Derecesi (IS): 70 ml suda çözünmüş olarak bulunan sertlik veren maddelerin, 1 mg kalsiyum karbonat(CaCO3) miktarına karşılık gelen madde miktarına denir. 0e sembolü ile gösterilir.
Alman Sertlik Derecesi (AS): 100 ml suda çözünmüş olarak bulunan sertlik veren maddelerin, 1mg kalsiyum oksit (CaO) miktarına karşılık gelen madde miktarına denir . 0dH sembolü ile gösterilir.
Sularda sertlik bu üç şekilde belirtilirse de genellikle Fransız sertlik derecesi kullanılır. Bu sertlik derecelerini birbirine çevirmek mümkündür.
Sertlik Derecelerine Göre Suların Sınıflandırılması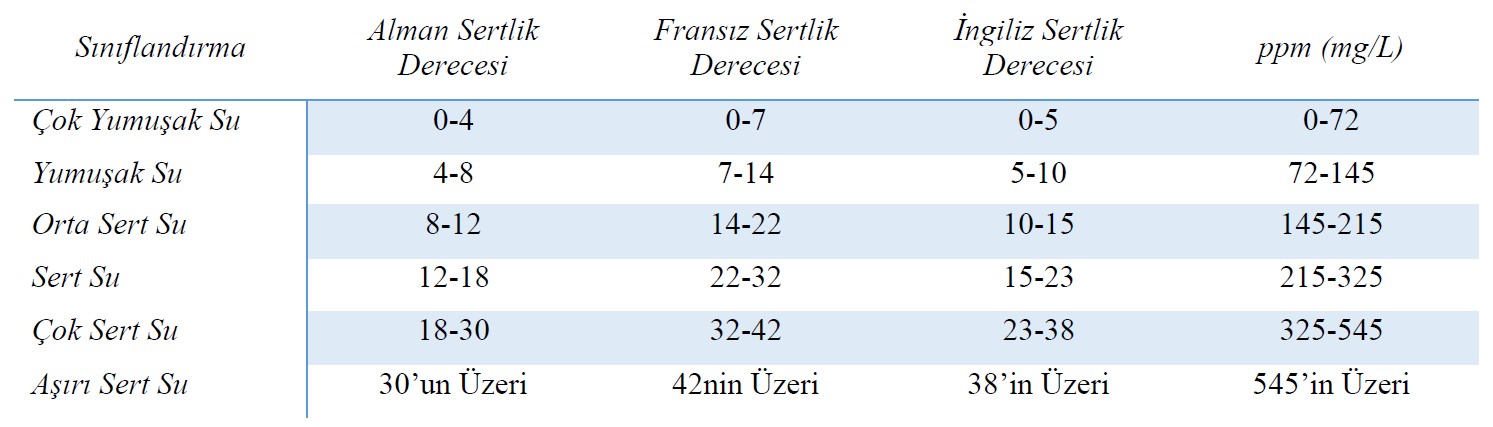
Sularda Sertlik Tayin Metotları
Sularda sertlik tayinleri üç aşamada yapılmaktadır. Sertlik bütününün bulunması, kalıcı sertliğin bulunması ve geçici sertliğin hesaplanması.
1- Sabun Metodu: Bu yöntem çok hassas bir yöntem değildir. Ancak pratik olması nedeniyle özellikle arazi analizleri ve sanayide uygulanır. Suya sertlik vererek köpürmesine engel olan Ca ve Mg gibi katyonların, ayarlı sabun çözeltisi ile çöktürülmesinden sonra suyun köpürtülmesiyle suyun toplam sertliğinin bulunması ilkesine dayanır.
EDTA Titrimetrik Metod: Suda çözünen toprak alkali metal tuzları katyonlarının (Ca+2 ve Mg+2) EDTA tuzları (Etilen diamin tetra asetik asit ve bunun disodyum tuzu) ile suda çözünebilen bileşik oluşturması ilkesine dayanır. Suyun toplam sertliği genellikle suda çözünmüş olarak bulunan kalsiyum ve magnezyum tuzlarından ileri gelir. Sudaki toplam Ca2+ ve Mg2+ iyonlarının bulunması yoluyla suyun sertliği belirlenebilir.
İçme ve Kullanma Sularının Sertlik Özellikleri
Herhangi bir suyun sabunun köpürmesine engel olan özelliğine suların sertliği denir.
Sertlik Çeşitleri
- Geçici sertlik
- Kalıcı sertlik
- Toplam sertlik olmak üzere üçe ayrılır.
1-Geçici Sertlik (Karbonat Sertliği): Kalsiyum ve magnezyum iyonlarının suda çözünmüş olan bikarbonatlarından ileri gelir.Suyun belirli bir süre kaynatılmasıyla sudaki kalsiyum ve magnezyum iyonları, çöktürülerek uzaklaştırıldığı için (CO2’de uçar ) geçici sertlik adı verilmiştir.
2-Kalıcı Sertlik (Karbonat Olamayan Sertlik): Kalsiyum ve magnezyum iyonlarının sülfat (SO4– ), klorür (Cl– ) ve nitrat 3 (NO3) iyonlarının oluşturduğu tuzların meydana getirdiği sertliktir. Bu tuzlar suda çözünmezler.
3- Toplam Sertlik (Sertlik Bütünü): Geçici ve kalıcı sertliğin toplamına denir.
Toplam Sertlik= Geçici Sertlik+ Kalıcı Sertlik
Kaynak: MEGEP Milli Eğitim Yayınları